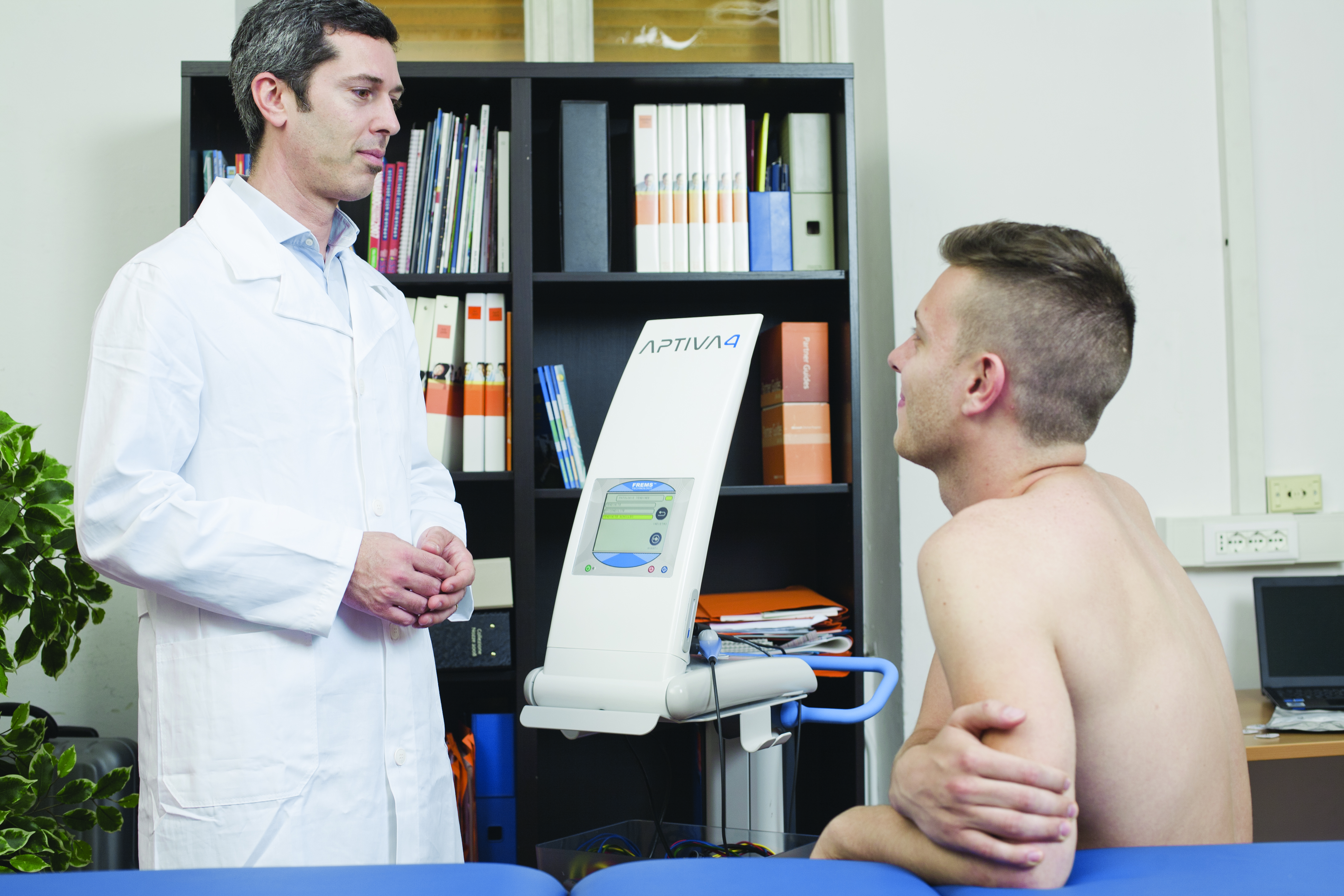
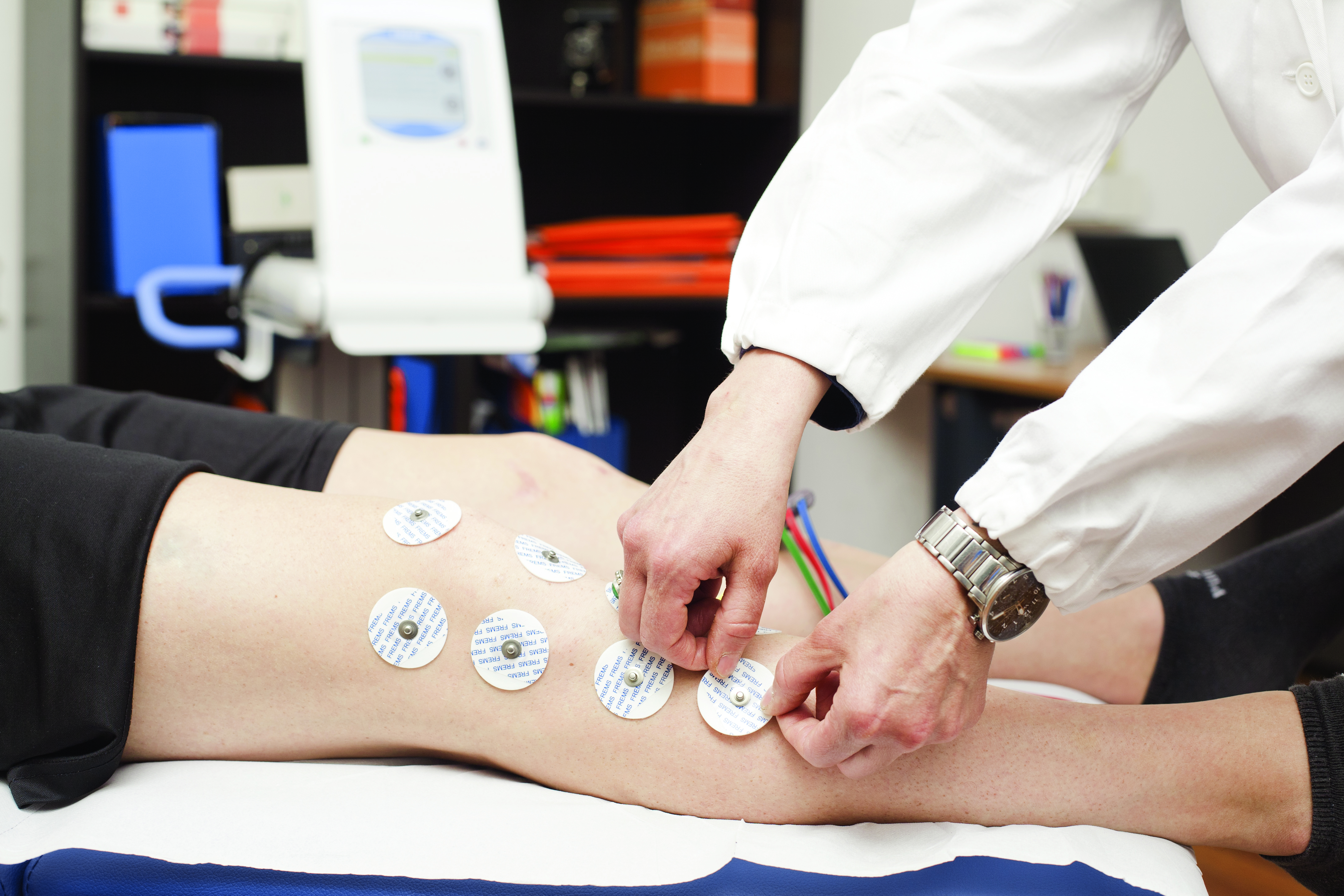
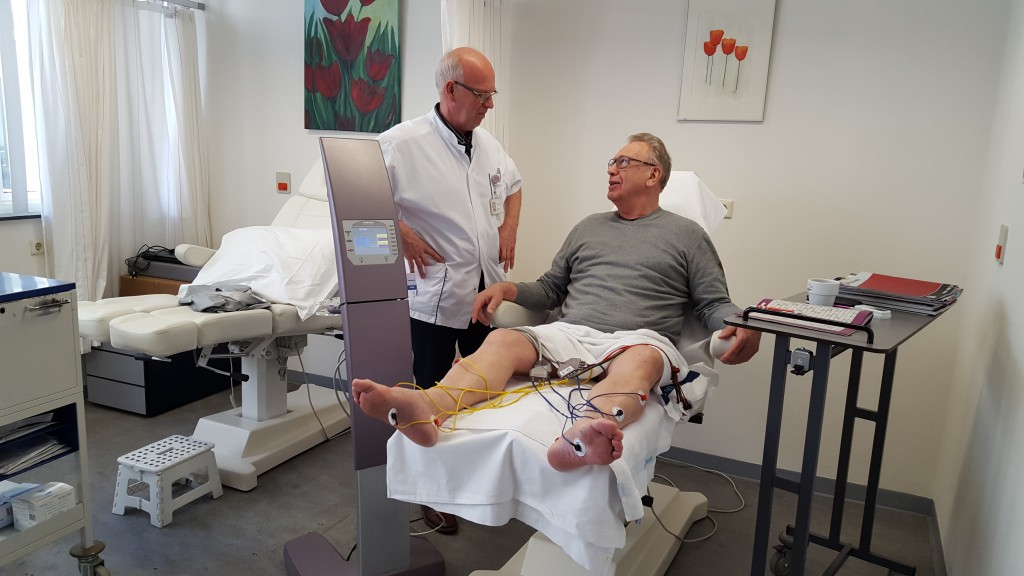
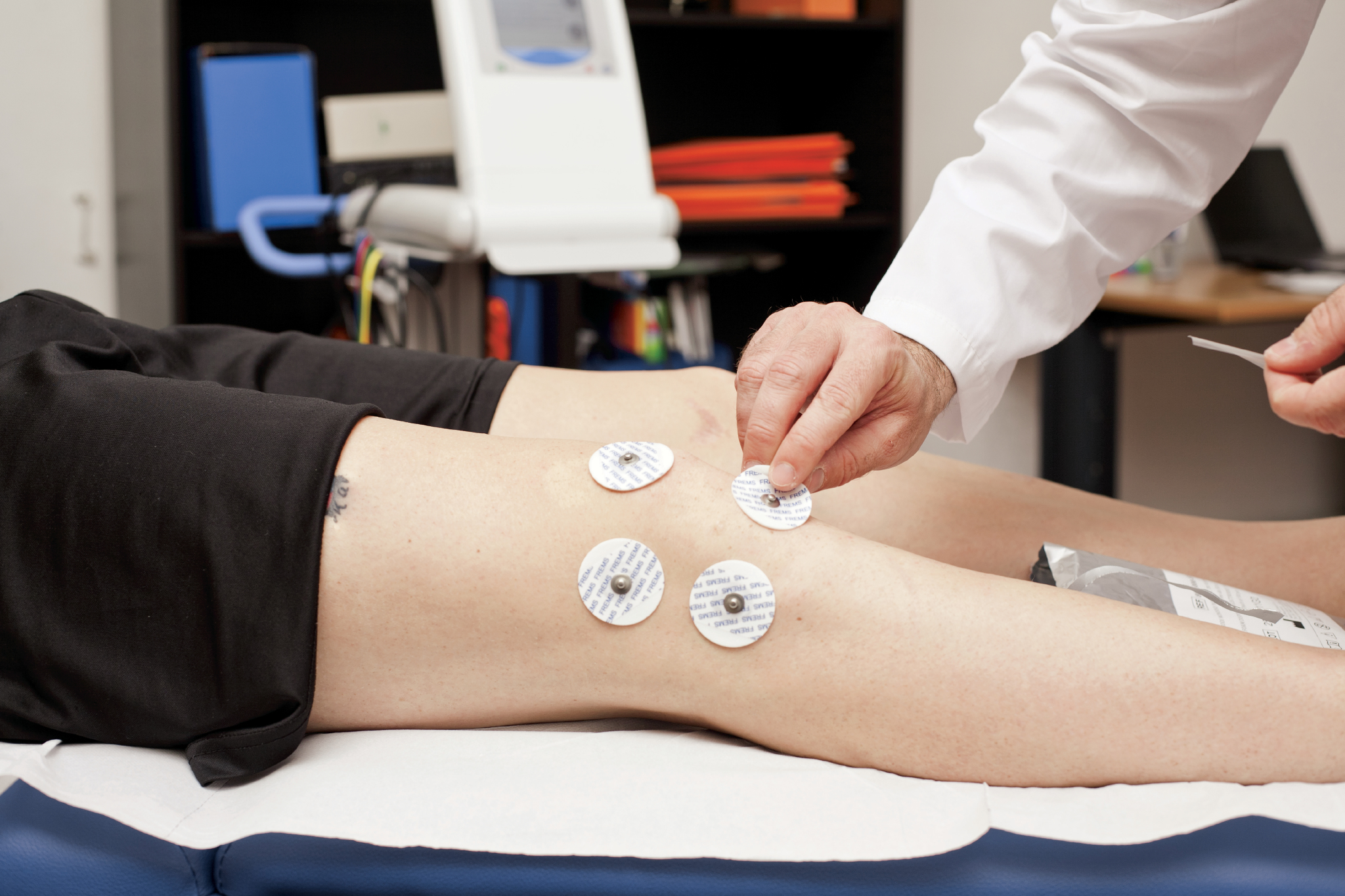
Voor het juiste begrip van FREMS is het van belang om de verschillen uiteen te zetten tussen deze methode en een andere bekende transcutane elektrische stimulatiemethode zijnde TENS (Transcutane Elektrische Zenuw Stimulatie).
De effecten van elektrische stimulatie bij TENS worden vanuit de Poorttheorie toegeschreven aan feitelijke beïnvloeding op de zenuwbanen zelf. De elektrische impulsen verhinderen dat pijnsignalen de hersenen bereiken, waardoor het gevoel van pijn wordt verlicht. Bij deze vorm van neurostimulatie treedt geen genezend effect op, echter slechts een een vermindering van de symptomen voor de duur van de behandeling.
De werking van FREMS, die essentieel verschilt van TENS, vindt zijn oorsprong in bevindingen uit fundamenteel experimenteel onderzoek.
In 2001 werd bij hamsters aangetoond dat (locale) elektrische activatie van endotheel met een negatieve puls leidde tot een langdurige vasodilatatie van de gehele arterie [1]. Daarnaast zijn er klassieke observaties van pre-angionetische responses van VEGF receptoren na elektrische stimulatie [2]. Hiermee lijkt elektrische stimulatie een primair vasculaire respons op te wekken hetgeen de curatieve toepassing van FREMS begrijpelijk maakt.
Ook al heeft FREMS een overlap met de klassieke TENS en zijn TENS-gelijke effecten aangetoond [3], de curatieve werking is met name gebaseerd op de hierboven genoemde vasculaire effecten van de FREMS behandeling.
FREMS kenmerkt zich verder door het intermitterende verloop van de behandeling, daar waar de TENS een chronische behandeling is. Binnen het behandelprotocol vinden 10 sessies in 2 weken plaats, waarna een voortdurend effect wordt waargenomen [5].
FREMS kenmerkt zich door sequenties van elektrische impulsen van korte duur (spikes) met een minimale stroomsterkte (orde mA) die variëren in frequentie en duur volgens vastgelegde protocollen. Kenmerkend is de negatieve spike die in staat is om vrije kleine zenuweinden te stimuleren (zogenaamde beta en delta uiteinden, gelegen in- en onderhuids).
Elektrische stimulatie is een universele manier van beïnvloeding van biologische functies. Indien een adequate elektrische stimulatie wordt toegediend kan door de huid ten gevolge van deze stimulatie (met nauwkeurige bepaalde ritmes en sequenties die variëren in tijd en frequentie) een interactie aan worden gegaan met cutane receptoren zoals aanraking, temperatuur etc. Daarnaast vindt interactie plaats met de niet gemyeliniseerde vrije cutane zenuweinden die betrokken zijn bij o.a. temperatuur, diffuse pijn en ontsteking en metabole mediatoren. FREMS heeft tevens aangetoonde interactie met gladde spiercellen van vasculair myoepitheel en dieper gelegen dwarsgestreept spiervezels. FREMS heeft haar effect door een directe en indirecte beïnvloeding van (autonome) biologische controle systemen.
Beïnvloeding van biologische processen:
Tijdens de FREMS behandeling is verandering van de microcirculatie aangetoond. Met Laser Doppler Flowmetingen is een toegenomen vasomotor activiteit waargenomen, zelfs bij aangetoonde autonome dysfunctie in type 2 DM (3).
Door adrenerge en niet-adrenerge vasomotor stimulatie neemt de O2 spanning in weefsels toe alsook de CO2 reductie passend bij verbeterde microcirculatie. Klassieke observaties van pre-angionetische responses door electrische stimulatie middels stimulatie van VEGF receptoren (2) werden door Bevilacua et al bevestigd na FREMS stimulatie in diabetische polyneuropathie (4). Tijdens FREMS is een snelle toename van diverse plasma groeifactoren waargenomen in bloed monsters, genomen elders dan de stimulatie site. Spiegels Vascular Endothelial Growth Factor (VEGF) en basic-Fibroblast Growth Factor (b-FGF) stijgen duidelijk al tijdens FREMS. In dezelfde studie werd aangetoond dat een stimulatie met TENS geen verandering gaf van deze groeifactoren (4).
Tot slot is een anti-imflammatoire respons door FREMS waargenomen; afname van TNF-a en IL-2 spiegels waren zichtbaar tot 1 maand na starten van de FREMS behandeling (FREMS applicatie folder, figuur bijgevoegd).
Weefsel herstel:
Juist de bovengenoemde groeifactoren, die ook angiogenese stimuleren, dragen bij aan toegenomen weefsel herstel. Verbeterde vascularisatie vermindert ischemie. Ook door beïnvloeding van spiertonus ten gevolge van de modulerende functies op efferente motorzenuw activiteit neemt weefselherstel toe.
Pijn beïnvloeding:
De beïnvloeding door bovengenoemde fenomenen en de inductie van functioneel refractaire periode van de neuronen van de spinale ganglia (zoals in alle elektrische stimulatie, vergelijk TENS) geeft een duaal effect en daarmee de grotere effectiviteit van FREMS bij onder andere Diabetische Neuropathie.
Specifieke toepassing bij Diabetes:
In een relatief kleine groep van 31 patiënten met ernstige Diabetische Neuropathie (DN) werd in Diabetologia 2005 de eerste ervaringen van de FREMS bij DN beschreven (5). In een gerandomiseerde, double-blind, cross-over opzet werd duidelijk dat alleen na de effectieve FREMS behandeling een verandering in de Visual Analogue Scale (VAS) pijnscore zichtbaar werd. Aangezien alle patiënten door de cross-over opzet altijd een effectieve FREMS behandeling kregen kon ook het effect na 4 maanden follow-up worden geëvalueerd. Duidelijk was dat het directe pijnverlagende effect na FREMS ook nog tot 4 maanden na aanvang van de studie voortduurde. Ook werd na 4 maanden een significante verandering gezien in Quality of Life (Q.O.L) parameters zoals Physical Functioning en General Mental Health (Table 3; p 820, artikel).
In een recente internationale multicenterstudie zijn 110 patiënten een jaar gevolgd in een dubbelblind gerandomiseerde opzet waarin patiënten drie behandelcycli ontvingen (6). De effecten van FREMS op de pijnscores overdag en ‘s nachts namen significant af van dag 1 naar dag 10 van de behandeling. In de periode tot aan het begin van de volgende behandeling verdween dit verschil om daarna weer duidelijk af te nemen tijdens de volgende FREMS behandeling. In de groep van FREMS behandelde patiënten had 50% een afname van minstens 50% pijn.
In 2011-2012 vond in het Tweestedenziekenhuis een Fase IV toepasbaarheidsonderzoek plaats van FREMS bij refractaire diabetische neuropathie. Onderzoekers zagen 1 maand na de behandeling een pijnafname van > 50% bij ruim 1/3 van de onderzochte groep van 70 patiënten (7). Dit heeft geleid tot een vervolgstudie, waarbij 220 patiënten in een periode van een jaar drie behandelcycli kregen. De twee laatstgenoemde onderzoeken zijn in 2016 gepresenteerd tijdens het congres van de American Diabetes Association (ADA) (8,9).
Referenties:
(voor de volledige bibliografie klik hier)
1) Emerson GG and Segal SS. Electrical activation of endothelium evokes vasodilatation and hyperpolarization along hamster feed arteries. Am. J. Physiol. Heart Circ. Physiol 2001:280:H160-H167.
2) Min Zhao, Huai Bai, Entong Wang, John V. Forrester and Colin D. McCaig. Electrical stimulation directly induces pre-angiogenic responses in vascular endothelial cells by signaling through VEGF receptors.J of Cell Science 2004;117:397-405
3) Bocchi L, Evangelisti A, Barella M, Scatizzi L, Bevilacua M.Recovery of 0,1 Hz microvascular skin flow in dysautonomic diabetic (type 2) neuropathy by using Frequency Rhytmic Electrical Modulation System (FREMS). Med Eng Phys (2010), doi:10.1016/j.medengphy.2010.02.004
4) Bevilacqua, M. Dominguez LJ, Barella M and Barbagallo M. Induction of vascular endothelial growth factor release by transcutaneous frequency modulated neural stimulation in diabetic polyneuropathy. J. Endocrinol. Invest. 2007;30:944-947.5) Bosi E, Conti M, Vermigli C et al. Effectiveness of frecuency-modulated electromagnetic neural stimulation in the treatment of painful diabetic neuropathy. Diabetologia 2005;48:817-823.
5) Bosi E, Conti M, Vermigli C et al. Effectiveness of frecuency-modulated electromagnetic neural stimulation in the treatment of painful diabetic neuropathy. Diabetologia 2005;48:817-823.`
6) Bosi, E, Bax, G Scionti, L et al. Frequency-modulated electromagnetic neural stimulation (FREMS) as a treatment for symptomatic diabetic neuropathy: results from a double-blind, randomised, multicentre, long-term, placebo-controlled clinical trial Diabetologia. 2013 March; 56(3): 467–475
7) J. Heijster, A. van der Ven, B. Imholz FREMS: meerwaarde bij refractaire diabetische neuropathie? Nederlands Tijdschrift voor Diabetologie 11-3 p17
8) Ben lmholz, Jack Heijster: Electrostimulation with EVNS is effective in therapy-refractory painful Diabetic Neuropathy. American Diabetes Association, 76th scientific sessions, June 201 6, New Orleans, LA
9) Ben lmholz, Jack Heijster: EVNS for painful Diabetic Neuropathy; results of repeated treatments during one year of follow-up. American Diabetes Association, 76th scientific sessions, June 2016, New Orleans, LA
–